कार्बनिक यौगिकों को दो मुख्य संरचनात्मक विशेषताओं के आधार पर वर्गीकृत किया जाता है:
कार्बन श्रृंखला (कार्बन कंकाल) की संरचना;
कार्यात्मक समूहों की उपस्थिति और संरचना।
कार्बन कंकाल (कार्बन श्रृंखला) रासायनिक रूप से बंधे हुए कार्बन परमाणुओं का एक क्रम है।
कार्यात्मक समूह - एक परमाणु या परमाणुओं का एक समूह जो एक निश्चित वर्ग के यौगिक से संबंधित होता है और इसके रासायनिक गुणों के लिए जिम्मेदार होता है।
कार्बन श्रृंखला की संरचना द्वारा यौगिकों का वर्गीकरण
कार्बन श्रृंखला की संरचना के आधार पर, कार्बनिक यौगिकों को चक्रीय और चक्रीय में विभाजित किया जाता है।
एसाइक्लिक यौगिक - यौगिकों के साथ खुला हुआ (open) कार्बन चेन। इन कनेक्शनों को भी कहा जाता है एलिफैटिक।
चक्रीय यौगिकों में, सीमित (संतृप्त) लोगों को प्रतिष्ठित किया जाता है, जिसमें कंकाल और केवल एकल सी-सी बॉन्ड होते हैं असंतृप्त (असंतृप्त), जिसमें कई बांड C \u003d C और C C शामिल हैं।
चक्रीय यौगिक
सीमा:

असीमित:

एसाइक्लिक यौगिकों को भी असंक्रमित और शाखित श्रृंखला यौगिकों में वर्गीकृत किया जाता है। इस मामले में, अन्य कार्बन परमाणुओं के साथ एक कार्बन परमाणु के बॉन्ड की संख्या को ध्यान में रखा जाता है।
श्रृंखला, जिसमें तृतीयक या चतुर्धातुक कार्बन परमाणु शामिल हैं, को शाखित किया जाता है (नाम में इसे अक्सर उपसर्ग "आइसो" द्वारा दर्शाया जाता है)।
उदाहरण के लिए:

कार्बन परमाणु:
प्राथमिक;
माध्यमिक;
तृतीयक।
चक्रीय यौगिक एक बंद कार्बन श्रृंखला के साथ यौगिक होते हैं।
चक्र को बनाने वाले परमाणुओं की प्रकृति के आधार पर, कार्बोकाइक्लिक और हेट्रोसाइक्लिक यौगिकों को प्रतिष्ठित किया जाता है।
कार्बोकाइक्लिक यौगिकों में रिंग में केवल कार्बन परमाणु होते हैं। उन्हें दो समूहों में विभाजित किया जाता है जो रासायनिक गुणों में काफी भिन्न होते हैं: एलीफेटिक चक्रीय - संक्षिप्त एलिसिलिक - और सुगंधित यौगिक।
कार्बोसायक्लिक यौगिक
Aliceclic:

सुगंधित:

हिटरोसायक्लिक यौगिकों में चक्र में होते हैं, कार्बन परमाणुओं के अलावा, अन्य तत्वों के एक या अधिक परमाणु होते हैं - heteroatoms (ग्रीक से heteros- अन्य, अलग) - ऑक्सीजन, नाइट्रोजन, सल्फर, आदि।
विषमकोण यौगिक

कार्यात्मक समूहों द्वारा यौगिकों का वर्गीकरण
ऐसे यौगिक जिनमें केवल कार्बन और हाइड्रोजन होते हैं, हाइड्रोकार्बन कहलाते हैं।
अन्य, अधिक कई, कार्बनिक यौगिकों को हाइड्रोकार्बन के डेरिवेटिव के रूप में माना जा सकता है, जो तब बनते हैं जब अन्य तत्वों वाले कार्यात्मक समूहों को हाइड्रोकार्बन में पेश किया जाता है।
कार्यात्मक समूहों की प्रकृति के आधार पर, कार्बनिक यौगिकों को कक्षाओं में विभाजित किया जाता है। कुछ सबसे विशिष्ट कार्यात्मक समूहों और यौगिकों के संबंधित वर्गों को तालिका में दिखाया गया है:
कार्बनिक यौगिकों की कक्षाएं

नोट: कार्यात्मक समूहों में कभी-कभी दोहरे और ट्रिपल बांड शामिल होते हैं।
कार्बनिक यौगिकों के अणुओं में दो या अधिक समान या विभिन्न कार्यात्मक समूह हो सकते हैं।
उदाहरण के लिए: HO - CH 2 - CH 2 - OH (एथिलीन ग्लाइकॉल); NH 2 -CH 2 - COOH (अमीनो एसिड) ग्लाइसिन).
कार्बनिक यौगिकों के सभी वर्ग परस्पर जुड़े हुए हैं। कार्बन कंकाल को बदले बिना यौगिकों के एक वर्ग से दूसरे में संक्रमण मुख्य रूप से कार्यात्मक समूहों के परिवर्तन के माध्यम से किया जाता है। प्रत्येक वर्ग के यौगिक एक समरूप श्रृंखला का निर्माण करते हैं।
अकार्बनिक से कार्बनिक रसायन के संक्रमण में, कोई यह पता लगा सकता है कि कार्बनिक और अकार्बनिक पदार्थों का वर्गीकरण कैसे भिन्न होता है। कार्बनिक यौगिकों की दुनिया में उनके विभिन्न प्रकार और विविधताएं हैं। कार्बनिक पदार्थों का वर्गीकरण न केवल इस बहुतायत को समझने में मदद करता है, बल्कि उनके अध्ययन के लिए एक स्पष्ट वैज्ञानिक आधार भी प्रदान करता है।
रासायनिक संरचना के सिद्धांत को कक्षाओं में वर्गीकरण के लिए आधार के रूप में चुना गया था। कार्बनिक पदार्थों के अध्ययन का आधार सबसे अधिक वर्ग के साथ काम है, जिसे आमतौर पर कार्बनिक पदार्थों के लिए मुख्य कहा जाता है - हाइड्रोकार्बन। जैविक दुनिया के अन्य प्रतिनिधियों को उनके डेरिवेटिव के रूप में माना जाता है। दरअसल, जब उनकी संरचना का अध्ययन करते हैं, तो यह नोटिस करना मुश्किल नहीं है कि इन पदार्थों का संश्लेषण एक (प्रतिस्थापित) करके, और कभी-कभी कई, हाइड्रोकार्बन संरचना में हाइड्रोजन इकाइयों अन्य रासायनिक तत्वों के परमाणुओं के साथ होता है, और कभी-कभी पूरी शाखाओं-कट्टरपंथी के साथ होता है।
कार्बनिक पदार्थों के वर्गीकरण ने हाइड्रोकार्बन को उनकी संरचना की सादगी के कारण भी एक आधार के रूप में लिया, और हाइड्रोकार्बन घटक ज्ञात कार्बनिक यौगिकों में से अधिकांश का सबसे महत्वपूर्ण हिस्सा है। आज तक, दुनिया से संबंधित सभी ज्ञात जीवों में, आधार पर निर्मित यौगिकों का एक महत्वपूर्ण प्रबलता है। अन्य सभी पदार्थ या तो अल्पमत में हैं, उन्हें सामान्य नियम के अपवाद के रूप में वर्गीकृत किया जा सकता है, या वे इतने अस्थिर हैं कि उनका उत्पादन हमारे समय में भी मुश्किल है।
अलग-अलग समूहों और वर्गों में विभाजन द्वारा कार्बनिक पदार्थों का वर्गीकरण दो बड़े कार्बनिक वर्गों के चक्रीय और चक्रीय यौगिकों को भेद करना संभव बनाता है। उनका बहुत नाम हमें अणु की संरचना के प्रकार के बारे में एक निष्कर्ष निकालने की अनुमति देता है। पहले मामले में, यह हाइड्रोकार्बन लिंक की एक श्रृंखला है, और दूसरे में, अणु एक अंगूठी है।
चक्रीय यौगिकों को शाखाओं में बँधाया जा सकता है या एक साधारण श्रृंखला बन सकती है। इन पदार्थों के नामों में अभिव्यक्ति "वसायुक्त या स्निग्ध हाइड्रोकार्बन" पाई जा सकती है। वे कुछ कार्बन इकाइयों के बंधन के प्रकार के आधार पर सीमित हो सकते हैं (ईथेन, आइसोब्यूटेन, या असंतृप्त (एथिलीन, एसिटिलीन, आइसोप्रिन)।
चक्रीय यौगिकों से संबंधित कार्बनिक पदार्थों का वर्गीकरण उनके आगे के विभाजन को कार्बोकाइक्लिक के समूह और हेट्रोसायक्लिक हाइड्रोकार्बन के एक समूह में शामिल करता है।
कार्बोकाइक्लिक "रिंग" केवल कार्बन परमाणुओं से बना होता है। वे एलिसिलिक (संतृप्त और असंतृप्त) हो सकते हैं, साथ ही सुगंधित कार्बोक्जिलिक यौगिक भी हो सकते हैं। एलिसिलिक यौगिकों में, कार्बन श्रृंखला के दो छोर बस शामिल हो जाते हैं, जबकि सुगंधित यौगिकों की संरचना में एक तथाकथित बेंजीन रिंग होता है, जो उनके गुणों पर महत्वपूर्ण प्रभाव डालता है।
अन्य पदार्थों के परमाणुओं को हेट्रोसाइक्लिक पदार्थों में पाया जा सकता है, अक्सर नाइट्रोजन इस कार्य को करता है।
कार्बनिक पदार्थों के गुणों को प्रभावित करने वाला अगला घटक तत्व एक कार्यात्मक समूह की उपस्थिति है।
हैलोजेनेटेड हाइड्रोकार्बन के लिए, एक या कई हलोजन परमाणु एक कार्यात्मक समूह के रूप में कार्य कर सकते हैं। हाइड्रॉक्सिल समूहों की उपस्थिति के कारण अल्कोहल को उनके गुण मिलते हैं। एल्डिहाइड के लिए, एक विशेषता विशेषता एल्डिहाइड समूहों की उपस्थिति है, केटोन्स के लिए - कार्बोनिल समूह। कार्बोक्जिलिक अम्ल इसमें भिन्न होते हैं कि उनमें कार्बोक्सिल समूह होते हैं, और अमाइन में एक अमीनो समूह होता है। नाइट्रो यौगिकों की विशेषता एक नाइट्रो समूह की उपस्थिति से होती है।
हाइड्रोकार्बन के प्रकार, साथ ही साथ उनके गुणों की विविधता बहुत अलग प्रकार के संयोजन पर आधारित है। उदाहरण के लिए, एक अणु की संरचना में दो या अधिक समान और कभी-कभी विभिन्न कार्यात्मक समूह शामिल हो सकते हैं, जो इस पदार्थ (ग्लिसरीन) के विशिष्ट गुणों का निर्धारण करते हैं।
मुद्दे (कार्बनिक पदार्थों के वर्गीकरण) पर विचार करने के लिए, इस लेख के पाठ में निहित जानकारी के आधार पर एक तालिका आसानी से संकलित की जा सकती है जो बहुत स्पष्टता देगी।
सबसे सरल वर्गीकरण है कि सभी ज्ञात पदार्थों में विभाजित हैं अकार्बनिक और जैविक... जैविक पदार्थों में शामिल हैं हाइड्रोकार्बन और उनके डेरिवेटिव। अन्य सभी पदार्थ अकार्बनिक हैं।

अकार्बनिक पदार्थ रचना में विभाजित है सरल और जटिल.

साधारण पदार्थएक रासायनिक तत्व के परमाणुओं से मिलकर और धातुओं, गैर-धातुओं, महान गैसों में विभाजित होते हैं। जटिल पदार्थ विभिन्न तत्वों के परमाणुओं से बने होते हैं जो रासायनिक रूप से एक दूसरे से बंधे होते हैं।
संरचना और गुणों द्वारा जटिल अकार्बनिक पदार्थों को निम्नलिखित सबसे महत्वपूर्ण वर्गों में विभाजित किया गया है: ऑक्साइड, कुर्सियां, एसिड, एम्फोटेरिक हाइड्रॉक्साइड, लवण।
- आक्साइड दो रासायनिक तत्वों से मिलकर जटिल पदार्थ होते हैं, जिनमें से एक ऑक्सीकरण राज्य (-2) के साथ ऑक्सीजन होता है। ऑक्साइड के सामान्य सूत्र: ई एम ओ एन, जहां एम तत्व ई के परमाणुओं की संख्या है, और एन ऑक्सीजन परमाणुओं की संख्या है। ऑक्साइड, बदले में, नमक बनाने और गैर-नमक बनाने के रूप में वर्गीकृत किया जाता है। नमक बनाने वाले को मूल, एम्फोटेरिक, एसिडिक में विभाजित किया जाता है, जो क्रमशः आधारों, एम्फोटेरिक हाइड्रोक्साइड्स, एसिड के अनुरूप होता है।
- बुनियादी ऑक्साइड - ये ऑक्सीडेशन स्टेट्स +1 और +2 में मेटल ऑक्साइड हैं। इसमें शामिल है:
- पहले समूह के मुख्य उपसमूह के धातु आक्साइड ( क्षारीय धातु) ली - फादर
- दूसरे समूह के मुख्य उपसमूह के धातु ऑक्साइड Mg और क्षारीय पृथ्वी धातु) मिलीग्राम - रा
- सबसे कम ऑक्सीकरण राज्यों में संक्रमण धातु ऑक्साइड
- एसिड ऑक्साइडगैर-धातुओं के साथ S.O. अधिक +2 और धातुओं के साथ S.O. +5 से +7 (SO 2, SeO 2, P 2 O 5, As 2 O 3, CO 2, SiO 2, CrO 3 और Mn 2 O 7)। अपवाद: ऑक्साइड के लिए NO 2 और क्लो 2 वहाँ कोई इसी अम्लीय हाइड्रॉक्साइड हैं, लेकिन उन्हें अम्लीय माना जाता है।
- एम्फ़ोटेरिक ऑक्साइड- एम्फोटेरिक धातुओं द्वारा गठित एस.ओ. +2, + 3, + 4 (BeO, Cr 2 O 3, ZnO, Al 2 O 3, GeO 2, SnO 2 और PbO)।
- गैर-नमक बनाने वाले ऑक्साइड - CO + 1, +2 (CO, NO, N 2 O, SiO) के साथ गैर-धातुओं के ऑक्साइड।
- नींव धातु परमाणुओं और एक या अधिक हाइड्रॉक्सो समूहों (-OH) से मिलकर जटिल पदार्थ होते हैं। आधारों का सामान्य सूत्र: एम (ओएच) वाई, जहां वाई धातु एम के ऑक्सीकरण राज्य (आमतौर पर +1 और +2) के बराबर हाइड्रॉक्सो समूहों की संख्या है। गैसों को घुलनशील (क्षार) और अघुलनशील में विभाजित किया जाता है।
- एसिड- (अम्लीय हाइड्रॉक्साइड) हाइड्रोजन परमाणुओं से मिलकर जटिल पदार्थ होते हैं जिन्हें धातु के परमाणुओं और अम्लीय अवशेषों द्वारा प्रतिस्थापित किया जा सकता है। एसिड का सामान्य सूत्र: H x Ac, जहां Ac एक एसिड अवशेष (अंग्रेजी "एसिड" - एसिड से) है, x एसिड रेजिड्यू आयन के चार्ज के बराबर हाइड्रोजन परमाणुओं की संख्या है।
- एम्फ़ोटेरिक हाइड्रॉक्साइड्स जटिल पदार्थ होते हैं जो अम्ल के गुणों और क्षारों के गुणों को प्रदर्शित करते हैं। इसलिए, अम्फोटेरिक हाइड्रॉक्साइड के सूत्र एसिड के रूप में और आधार के रूप में दोनों लिखे जा सकते हैं।
- नमक धातु अवशेषों और एसिड अवशेषों के आयनों से मिलकर जटिल पदार्थ होते हैं। यह परिभाषा मध्यम नमक पर लागू होती है।
- मध्यम लवण धातु परमाणुओं द्वारा एक एसिड अणु में हाइड्रोजन परमाणुओं के पूर्ण प्रतिस्थापन के उत्पाद हैं या एसिड अवशेषों के साथ एक आधार अणु में हाइड्रॉक्सो समूहों का पूर्ण प्रतिस्थापन है।
- अम्लीय लवण - एसिड में हाइड्रोजन परमाणुओं को आंशिक रूप से धातु परमाणुओं द्वारा प्रतिस्थापित किया जाता है। वे एसिड की अधिकता के साथ आधार को बेअसर करके प्राप्त किए जाते हैं। सही ढंग से नाम के लिए खट्टा नमक एसिड नमक बनाने वाले हाइड्रोजन परमाणुओं की संख्या के आधार पर, सामान्य नमक के नाम के साथ उपसर्ग हाइड्रो- या डाइहाइड्रो को जोड़ना आवश्यक है। उदाहरण के लिए, केएचसीओ 3 पोटेशियम बाइकार्बोनेट, केएच 2 पीओ 4 पोटेशियम डाइहाइड्रोजेन फॉस्फेट है। यह याद रखना चाहिए कि अम्लीय लवण केवल दो या अधिक मूल एसिड बना सकते हैं।
- मूल लवण आधार के हाइड्रॉक्सिल समूह (OH -) अम्लीय अवशेषों द्वारा आंशिक रूप से प्रतिस्थापित किए जाते हैं। बुलाना मूल नमक, यह सामान्य नमक के नाम के उपसर्ग हाइड्रॉक्सो या डाइहाइड्रॉक्सो को जोड़ने के लिए आवश्यक है, जो नमक बनाने वाले ओएच - समूहों की संख्या पर निर्भर करता है। उदाहरण के लिए, (CuOH) 2 CO 3 - कॉपर (II) हाइड्रॉक्सीसाइक्लेट। यह याद रखना चाहिए कि मूल लवण केवल आधार बना सकते हैं। दो या अधिक हाइड्रॉक्सिल समूह युक्त।
- डबल साल्ट - इनमें दो अलग-अलग पिंजरे होते हैं, जो अलग-अलग उद्धरणों के साथ लवण के मिश्रित समाधान से क्रिस्टलीकरण द्वारा प्राप्त किए जाते हैं, लेकिन एक ही आयन होते हैं। उदाहरण के लिए, KAl (SO 4) 2, KNaSO 4।
- मिश्रित लवण - उनमें दो अलग-अलग आयन होते हैं। उदाहरण के लिए, सीए (OCl) Cl।
- हाइड्रेट लवण (क्रिस्टलीय हाइड्रेट्स)) - इनमें क्रिस्टलीकरण के पानी के अणु शामिल हैं। उदाहरण: Na 2 SO 4 10H 2 O

कार्बनिक पदार्थों का वर्गीकरण
केवल हाइड्रोजन और कार्बन परमाणुओं वाले यौगिकों को कहा जाता है हाइड्रोकार्बन... इस खंड को शुरू करने से पहले, याद रखें, लेखन को सरल बनाने के लिए, केमिस्ट कार्बन और हाइड्रोजेन की श्रृंखलाओं का वर्णन नहीं करते हैं, लेकिन यह मत भूलो कि कार्बन चार बॉन्ड बनाता है, और यदि आंकड़ा कार्बन दो बॉन्ड से जुड़ा हुआ है, तो दो और इसे हाइड्रोजेन से जोड़ा जाता है, हालांकि बाद वाला है। निर्दिष्ट नहीं है:

कार्बन श्रृंखला की संरचना के आधार पर, कार्बनिक यौगिकों को एक खुली श्रृंखला के साथ यौगिकों में विभाजित किया जाता है - अचक्रीय (एलीपेटिक) और चक्रीय - परमाणुओं की एक बंद श्रृंखला के साथ।
चक्रीय दो समूहों में विभाजित हैं: carbocyclic कनेक्शन और heterocyclic.
कार्बोसायक्लिक यौगिकबदले में, यौगिकों की दो श्रृंखला शामिल करें: ऐलीचक्रीय तथा खुशबूदार.
सुगंधित यौगिक अणुओं की संरचना--इलेक्ट्रॉनों की एक विशेष बंद प्रणाली के साथ फ्लैट कार्बन युक्त चक्रों पर आधारित है। एक सामान्य a-प्रणाली (एक एकल cloud-इलेक्ट्रॉन क्लाउड) बनाना।

दोनों चक्रीय (स्निग्ध) और चक्रीय हाइड्रोकार्बन में कई (डबल या ट्रिपल) बॉन्ड हो सकते हैं। ऐसे हाइड्रोकार्बन कहलाते हैं असंतृप्त(असंतृप्त), विपरीत सीमा(संतृप्त) जिसमें केवल एक बंधन हो।
पी-बॉन्ड (--बंधन) एक सहसंयोजक बंधन है जो पी-एटॉमिक ऑर्बिटल्स को ओवरलैप करके बनता है। सिग्मा बॉन्ड के विपरीत, जो परमाणु संबंध की रेखा के साथ एस-एटॉमिक ऑर्बिटल्स को ओवरलैप करके किया जाता है, पी-बॉन्ड ऑर्बिटल्स परमाणु बॉन्ड लाइन के दोनों ओर ओवरलैप करते हैं।
एक सुगंधित प्रणाली के गठन के मामले में, उदाहरण के लिए, बेंजीन C6H6, छह कार्बन परमाणुओं में से प्रत्येक sp2 की स्थिति में है - संकरण और 120 ° के बंधन कोण के साथ तीन सिग्मा बांड बनाता है। प्रत्येक कार्बन परमाणु का चौथा पी-इलेक्ट्रॉन बेंजीन वलय के समतल के लिए लंबवत है। सामान्य तौर पर, एक एकल बंधन प्रकट होता है, जो बेंजीन रिंग के सभी कार्बन परमाणुओं तक फैला होता है। सिग्मा बांड के विमान के दोनों किनारों पर उच्च इलेक्ट्रॉन घनत्व के पाई बांड के दो क्षेत्र बनते हैं। इस तरह के बंधन के साथ, बेंजीन अणु में सभी कार्बन परमाणु समतुल्य हो जाते हैं और इसलिए, इस तरह की प्रणाली तीन स्थानीयकृत दोहरे बांडों वाली प्रणाली की तुलना में अधिक स्थिर है।

संतृप्त स्निग्ध हाइड्रोकार्बन को एल्केन्स कहा जाता है, उनके पास सामान्य सूत्र C n H 2n + 2 है, जहां n कार्बन परमाणुओं की संख्या है। उनका पुराना नाम आजकल इस्तेमाल किया जाता है - पैराफिन:
एक तिहरे बंधन वाले असंतृप्त एलीफेटिक हाइड्रोकार्बन को एल्काइनस कहा जाता है। उनका सामान्य सूत्र C n H 2n - 2 है
संतृप्त एलिसिलिक हाइड्रोकार्बन साइक्लोकलेन हैं, उनका सामान्य सूत्र है С n Н 2n:

हमने हाइड्रोकार्बन के वर्गीकरण की समीक्षा की है। लेकिन अगर इन अणुओं में एक या एक से अधिक हाइड्रोजन परमाणुओं को परमाणुओं (हैलोजन, हाइड्रॉक्सिल समूह, अमीनो समूह, आदि) के अन्य परमाणुओं या समूहों द्वारा प्रतिस्थापित किया जाता है, तो हाइड्रोकार्बन डेरिवेटिव्स का निर्माण होता है: हैलोजन डेरिवेटिव, ऑक्सीजन युक्त, नाइट्रोजन युक्त और अन्य कार्बनिक यौगिक।

परमाणुओं के समूह या समूह जो किसी दिए गए वर्ग के सबसे विशिष्ट गुणों को निर्धारित करते हैं, उन्हें कार्यात्मक समूह कहा जाता है।
एक ही कार्यात्मक समूह के साथ उनके व्युत्पन्न में हाइड्रोकार्बन समरूप श्रृंखला बनाते हैं।
एक समरूप श्रृंखला एक ही वर्ग (समरूप) से संबंधित यौगिकों की एक श्रृंखला है, जो संरचना में एक दूसरे से भिन्न होती है -CH 2 - समूहों (समरूप अंतर) के पूर्णांक संख्या में, समान संरचना और इसलिए, समान रासायनिक गुण हैं।
Homologues के रासायनिक गुणों की समानता कार्बनिक यौगिकों के अध्ययन को बहुत सरल करती है।
स्थानापन्न हाइड्रोकार्बन
- हैलोजेनेटेड हाइड्रोकार्बन हलोजन परमाणुओं द्वारा एक या एक से अधिक हाइड्रोजन परमाणुओं के हाइड्रोकार्बन में प्रतिस्थापन के उत्पादों के रूप में माना जा सकता है। इसके अनुसार, सीमित और असंतृप्त मोनो-, ली-, ट्राई (आम तौर पर पॉली-) हैलोजेन डेरिवेटिव्स में मौजूद हो सकते हैं। हैलोजेनेटेड संतृप्त हाइड्रोकार्बन आर-जी के सामान्य सूत्र। ऑक्सीजन युक्त कार्बनिक पदार्थों में अल्कोहल, फिनोल, एल्डीहाइड, कीटोन, कार्बोक्जिलिक एसिड शामिल हैं। , पंख और एस्टर।
- अल्कोहल - हाइड्रोकार्बन के डेरिवेटिव जिसमें एक या एक से अधिक हाइड्रोजन परमाणुओं को हाइड्रॉक्सिल समूहों द्वारा प्रतिस्थापित किया जाता है। अल्कोहल के डेरिवेटिव होने पर अल्कोहल को मोनोआटोमिक कहा जाता है, और संतृप्त, यदि वे अल्केन्स के डेरिवेटिव हैं, तो संतृप्त मोनोहाइड्रिक अल्कोहल का सामान्य सूत्र: आर-ओएच।
- फिनोल - एरोमैटिक हाइड्रोकार्बन (बेंजीन श्रृंखला) के डेरिवेटिव, जिसमें बेंजीन रिंग में एक या अधिक हाइड्रोजन परमाणुओं को हाइड्रॉक्सिल समूहों द्वारा प्रतिस्थापित किया जाता है।
- एल्डिहाइड और किटोन - परमाणुओं के कार्बोनिल समूह (कार्बोनिल) वाले हाइड्रोकार्बन का व्युत्पन्न। एल्डिहाइड अणुओं में, कार्बोनिल का एक बंधन हाइड्रोजन परमाणु के साथ यौगिक में जाता है, दूसरा - हाइड्रोकार्बन मूलक के साथ। केटोन्स के मामले में, कार्बोनिल समूह दो (आम तौर पर अलग-अलग) मूलांक से जुड़ा होता है।
- ईथर एक कार्बनिक परमाणु द्वारा जुड़े दो हाइड्रोकार्बन कट्टरपंथी युक्त कार्बनिक पदार्थ हैं: आर \u003d ओ - आर या आर - ओ - आर 2. कट्टरपंथी एक ही या अलग हो सकते हैं। पंखों की संरचना C n H 2n + 2O सूत्र द्वारा व्यक्त की जाती है।
- एस्टर - कार्बोक्सिलिक एसिड में कार्बोक्सिल समूह के हाइड्रोजन परमाणु की जगह एक हाइड्रोकार्बन कट्टरपंथी के साथ गठित यौगिक।
- नाइट्रो यौगिक - हाइड्रोकार्बन का व्युत्पन्न जिसमें एक या एक से अधिक हाइड्रोजन परमाणुओं को नाइट्रो समूह द्वारा प्रतिस्थापित किया जाता है -कोई 2।
- amines - अमोनिया के डेरिवेटिव के रूप में माने जाने वाले यौगिक, जिसमें हाइड्रोजन परमाणुओं को हाइड्रोकार्बन रेडिकल्स द्वारा प्रतिस्थापित किया जाता है। रेडिकल की प्रकृति के आधार पर, एमाइन एलिफैटिक हो सकते हैं। कट्टरपंथी, प्राथमिक अमाइन, माध्यमिक और तृतीयक अमीन्स द्वारा प्रतिस्थापित हाइड्रोजन परमाणुओं की संख्या के आधार पर प्रतिष्ठित किया जाता है। किसी विशेष मामले में, द्वितीयक और तृतीयक अमाइन के मूलांक समान हो सकते हैं। प्राथमिक अमाइन को हाइड्रोकार्बन (अल्केन्स) के डेरिवेटिव के रूप में भी माना जा सकता है जिसमें एक हाइड्रोजन परमाणु को एक एमिनो समूह द्वारा प्रतिस्थापित किया जाता है। एमिनो एसिड में दो कार्यात्मक समूह होते हैं जो एक हाइड्रोकार्बन रेडिकल से जुड़े होते हैं, एक एमिनो समूह -NH 2 और एक कार्बोक्सिल -COOH।
अन्य महत्वपूर्ण कार्बनिक यौगिकों को जाना जाता है जिनमें कई अलग-अलग या समान कार्यात्मक समूह होते हैं, बेंजीन के छल्ले से जुड़ी लंबी रैखिक श्रृंखलाएं। ऐसे मामलों में, किसी विशेष वर्ग के लिए किसी पदार्थ से संबंधित एक सख्त परिभाषा असंभव है। इन यौगिकों को अक्सर पदार्थों के विशिष्ट समूहों में अलग किया जाता है: कार्बोहाइड्रेट, प्रोटीन, न्यूक्लिक एसिड, एंटीबायोटिक्स, अल्कलॉइड, आदि। वर्तमान में, ऐसे कई यौगिक भी हैं जिन्हें कार्बनिक और अकार्बनिक के रूप में वर्गीकृत किया जा सकता है। उन्हें ऑर्गेनोलेमेंट यौगिक कहा जाता है। उनमें से कुछ को हाइड्रोकार्बन के डेरिवेटिव के रूप में माना जा सकता है।
शब्दावली
कार्बनिक यौगिकों के नाम के लिए, 2 नामकरण का उपयोग किया जाता है - तर्कसंगत और व्यवस्थित (IUPAC) और तुच्छ नाम.

IUPAC नामकरण संकलन:
1) यौगिक के नाम का आधार मुख्य श्रृंखला के समान परमाणुओं के साथ एक संतृप्त हाइड्रोकार्बन को दर्शाने वाले शब्द की जड़ है।
2) एक प्रत्यय को संतृप्ति की डिग्री के मूल में जोड़ा जाता है:
एक (सीमित, कोई एकाधिक कनेक्शन);
योंग (एक दोहरे बंधन की उपस्थिति में);
यिंग (एक ट्रिपल बांड की उपस्थिति में)।

यदि कई कई बॉन्ड हैं, तो इस तरह के बॉन्ड की संख्या प्रत्यय (-dien, -triene, आदि) में इंगित की गई है, और प्रत्यय के बाद, कई बॉन्ड की स्थिति को संख्याओं में इंगित किया जाना चाहिए, उदाहरण के लिए:
СН 3-вН 2-вН \u003d СН 2 СН 3 -СН \u003d СН - СН 3
butene-1 butene-2
सीएच 2 \u003d सीएच - सीएच \u003d सीएच 2
नाइट्रो-, हैलोजेन, हाइड्रोकार्बन रेडिकल जैसे मुख्य श्रृंखला में शामिल नहीं किए जाने वाले समूह उपसर्ग में किए जाते हैं। हालांकि, वे वर्णानुक्रम में सूचीबद्ध हैं। स्थानापन्न की स्थिति उपसर्ग के सामने एक संख्या द्वारा इंगित की जाती है।
नाम की रचना का क्रम इस प्रकार है:
1. परमाणुओं C की सबसे लंबी श्रृंखला ज्ञात कीजिए।
2. मुख्य श्रृंखला के कार्बन परमाणुओं की संख्या, शाखा के निकटतम छोर से शुरू होती है।
3. अल्केन का नाम वर्णमाला के क्रम में सूचीबद्ध साइड रेडिकल्स के नामों से बना है, जो मुख्य श्रृंखला में स्थिति और मुख्य श्रृंखला के नाम को दर्शाता है।
 नाम क्रम
नाम क्रम रासायनिक भाषा, जिसमें रासायनिक चिह्न (रासायनिक सूत्र सहित) सबसे विशिष्ट भागों में से एक है, रसायन विज्ञान को समझने का एक महत्वपूर्ण सक्रिय साधन है और इसलिए इसे एक स्पष्ट और सचेत अनुप्रयोग की आवश्यकता है।
रासायनिक सूत्र रासायनिक प्रतीकों, सूचकांकों और अन्य संकेतों के माध्यम से रासायनिक रूप से व्यक्तिगत पदार्थों की संरचना और संरचना की पारंपरिक छवियां हैं। पदार्थों की संरचना, रासायनिक, इलेक्ट्रॉनिक और स्थानिक संरचना का अध्ययन करते समय, उनके भौतिक और रासायनिक गुण, समरूपता और अन्य घटनाएं, विभिन्न प्रकार के रासायनिक सूत्र का उपयोग किया जाता है।
विशेष रूप से कई प्रकार के सूत्र (सरलतम, आणविक, संरचनात्मक, प्रक्षेपण, उत्क्रमण आदि) आणविक संरचना के पदार्थों के अध्ययन में उपयोग किए जाते हैं - अधिकांश कार्बनिक पदार्थ और सामान्य परिस्थितियों में अकार्बनिक पदार्थों का अपेक्षाकृत छोटा हिस्सा। गैर-आणविक यौगिकों के अध्ययन में महत्वपूर्ण रूप से कम प्रकार के सूत्र (प्रोटोजोआ) का उपयोग किया जाता है, जिनमें से संरचना बॉल-रॉड मॉडल और क्रिस्टल संरचनाओं के आरेख या उनकी इकाई कोशिकाओं द्वारा अधिक स्पष्ट रूप से परिलक्षित होती है।

हाइड्रोकार्बन के पूर्ण और लघु संरचनात्मक सूत्रों का संकलन
उदाहरण:
प्रोपेन सी 3 एच 8 का पूर्ण और संक्षिप्त संरचनात्मक सूत्र बनाएं।
फेसला:
1. एक पंक्ति में 3 कार्बन परमाणुओं को लिखें, उन्हें बॉन्ड से जोड़ें:
सी - सी - सी
2. डैश (बॉन्ड) जोड़ें ताकि प्रत्येक कार्बन परमाणु से 4 बॉन्ड निकल जाएं:
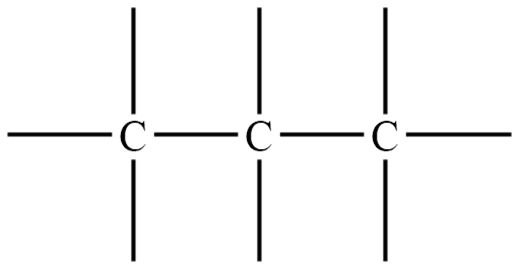

4. एक छोटे संरचनात्मक सूत्र को लिखें:
CH 3 -CH 2 -CH 3
घुलनशीलता तालिका
कार्बनिक पदार्थों का वर्गीकरण
कार्बन श्रृंखला की संरचना के प्रकार के आधार पर, कार्बनिक पदार्थों को विभाजित किया जाता है:
- चक्रीय और चक्रीय।
- सीमित (संतृप्त) और असंतृप्त (असंतृप्त)।
- कार्बोसायक्लिक और हेट्रोसाइक्लिक।
- एलिसिलिक और सुगंधित।
अकार्बनिक यौगिक अणुओं में कार्बनिक यौगिक होते हैं जिनमें कोई चक्र नहीं होते हैं और सभी कार्बन परमाणु एक दूसरे से सीधे या शाखित खुली श्रृंखलाओं से जुड़े होते हैं।
बदले में, चक्रीय यौगिकों के बीच, सीमित (या संतृप्त) वालों को प्रतिष्ठित किया जाता है, जो कार्बन कंकाल में केवल कार्बन-कार्बन (सी-सी) बांड और असंतृप्त (या असंतृप्त) होते हैं, जिसमें कई (डबल \u003d सी) या ट्रिपल (C≡) होते हैं ग) संचार।
चक्रीय यौगिक रासायनिक यौगिक होते हैं जिनमें एक रिंग बनाने के लिए तीन या अधिक बंधे हुए परमाणु होते हैं।
जिसके आधार पर परमाणुओं के छल्ले बनते हैं, कार्बोक्जिलिक यौगिक और हेट्रोसाइक्लिक यौगिकों को प्रतिष्ठित किया जाता है।
कार्बोकाइक्लिक यौगिकों (या आइसोसाइक्लिक) में उनके छल्ले में केवल कार्बन परमाणु होते हैं। ये यौगिक, बदले में, एलिसिलिक यौगिकों (एलीफेटिक साइक्लिक) और सुगंधित यौगिकों में विभाजित होते हैं।
हेटरोसाइक्लिक यौगिकों में हाइड्रोकार्बन रिंग में एक या अधिक हेटरोआटम्स होते हैं, जिनमें अक्सर ऑक्सीजन, नाइट्रोजन या सल्फर के परमाणु होते हैं।
कार्बनिक पदार्थों का सबसे सरल वर्ग हाइड्रोकार्बन है - यौगिक जो कार्बन और हाइड्रोजन परमाणुओं द्वारा विशेष रूप से बनते हैं, अर्थात्। औपचारिक रूप से कार्यात्मक समूह नहीं हैं।
चूंकि हाइड्रोकार्बन में कार्यात्मक समूह नहीं होते हैं, केवल कार्बन कंकाल के प्रकार से वर्गीकरण संभव है। हाइड्रोकार्बन, उनके कार्बन कंकाल के प्रकार के आधार पर, उपवर्गों में विभाजित होते हैं:
1) संतृप्त अम्लीय हाइड्रोकार्बन को अल्केन्स कहा जाता है। अल्केन्स का सामान्य आणविक सूत्र C n H 2n + 2 के रूप में लिखा जाता है, जहाँ n एक हाइड्रोकार्बन अणु में कार्बन परमाणुओं की संख्या है। इन यौगिकों में कोई इंटरक्लास आइसोमर्स नहीं है।
2) अम्लीय असंतृप्त हाइड्रोकार्बन में विभाजित हैं:
क) एलिकेंस - उनमें केवल एक ही मल्टीपल होता है, जिसका नाम है एक डबल सी \u003d सी बॉन्ड, एलकेन्स का सामान्य फॉर्मूला है C n 2 H,
बी) एल्केनीज - एल्काइनों के अणुओं में केवल एक ही मल्टीपल, अर्थात् ट्रिपल CC बॉन्ड है। एल्केनीज़ सी एन एच 2 एन -2 का सामान्य आणविक सूत्र
ग) एल्केडियन - एल्केडियन अणुओं में दो डबल सी \u003d सी बॉन्ड होते हैं। एल्केडिएन्स सी एन एच 2 एन -2 का सामान्य आणविक सूत्र
3) चक्रीय संतृप्त हाइड्रोकार्बन को साइक्लोकलेन कहा जाता है और इसमें सामान्य आणविक सूत्र C n H 2n होता है।
कार्बनिक रसायन विज्ञान के बाकी कार्बनिक पदार्थों को हाइड्रोकार्बन के डेरिवेटिव के रूप में माना जाता है, जब तथाकथित कार्यात्मक समूह, जिसमें अन्य रासायनिक तत्व होते हैं, हाइड्रोकार्बन अणुओं में पेश किए जाते हैं।
इस प्रकार, एक कार्यात्मक समूह वाले यौगिकों को आर-एक्स के रूप में लिखा जा सकता है, जहां आर एक हाइड्रोकार्बन कट्टरपंथी है, और एक्स एक कार्यात्मक समूह है। एक हाइड्रोकार्बन कट्टरपंथी एक या अधिक हाइड्रोजन परमाणुओं के बिना किसी भी हाइड्रोकार्बन के अणु का एक टुकड़ा है।
कुछ कार्यात्मक समूहों की उपस्थिति के अनुसार, यौगिकों को कक्षाओं में विभाजित किया जाता है। यौगिकों के मुख्य कार्यात्मक समूह और कक्षाएं, जिनमें उन्हें शामिल किया गया है, उन्हें तालिका में प्रस्तुत किया गया है:

इस प्रकार, विभिन्न कार्यात्मक समूहों के साथ कार्बन कंकाल के प्रकार के विभिन्न संयोजन कार्बनिक यौगिकों के विभिन्न प्रकार प्रदान करते हैं।
हैलोजेनेटेड हाइड्रोकार्बन
हैलोजेनेटेड हाइड्रोकार्बन किसी भी हैलोजन के क्रमशः एक या अधिक परमाणुओं के साथ किसी भी शुरुआती हाइड्रोकार्बन के अणु में एक या एक से अधिक हाइड्रोजन परमाणुओं को प्रतिस्थापित करके प्राप्त यौगिक हैं।
चलो कुछ हाइड्रोकार्बन का सूत्र है सी एन एच एम, तब जब इसके अणु में प्रतिस्थापित किया जाता है एक्स हाइड्रोजन परमाणु प्रति एक्स हलोजन परमाणु, हलोजन व्युत्पन्न के लिए सूत्र होगा सी एन एच एम- एक्स हाल एक्स ... इस प्रकार, अल्केन्स के मोनोक्र्लोरो डेरिवेटिव का सूत्र है सी एन एच 2 एन + 1 सीएल, डिक्लोरो डेरिवेटिव सी एन एच 2 एन क्ल 2 आदि।
अल्कोहल और फिनोल
अल्कोहल - हाइड्रोकार्बन का व्युत्पन्न, एक या अधिक हाइड्रोजन परमाणु जिसमें हाइड्रॉक्सिल समूह -OH द्वारा प्रतिस्थापित किया जाता है। एक हाइड्रॉक्सिल समूह वाली शराब को कहा जाता है मोनोएटोमिक, के साथ दो - दो परमाणुओंवाला, तीन के साथ triatomic आदि। उदाहरण के लिए:
दो या दो से अधिक हाइड्रॉक्सिल समूहों वाली शराब को भी कहा जाता है पॉलीहाइड्रिक अल्कोहल।संतृप्त मोनोहाइड्रिक अल्कोहल का सामान्य सूत्र सी एन एच 2 एन + 1 ओएच या सी एन एच 2 एन + 2 ओ। संतृप्त पॉलीहाइड्रिक अल्कोहल का सामान्य सूत्र सी एन एच 2 एन + 2 ओ एक्स, जहां एक्स अल्कोहल की परमाणुता है।
अल्कोहल भी खुशबूदार हो सकते हैं। उदाहरण के लिए:
बेंजाइल अल्कोहलऐसे मोनोहाइड्रिक सुगंधित अल्कोहल का सामान्य सूत्र C n H 2n-6 O है।
हालांकि, यह स्पष्ट रूप से समझा जाना चाहिए कि खुशबूदार हाइड्रोकार्बन डेरिवेटिव जिसमें हाइड्रोक्सील समूह सुगंधित नाभिक में एक या अधिक हाइड्रोजन परमाणुओं द्वारा प्रतिस्थापित किए जाते हैं लागू न करें शराब के लिए। वे वर्ग के हैं फिनोल ... उदाहरण के लिए, यह दिया गया यौगिक अल्कोहल है:
और यह फिनोल है:
फ़ेनॉल्स को अल्कोहल के रूप में वर्गीकृत नहीं किया जाता है, यह उनके विशिष्ट रासायनिक गुणों के कारण है, जो अल्कोहल से बहुत अलग हैं। यह देखना आसान है कि मोनोहाइड्रिक फेनोल्स मोनोहाइड्रिक एरोमैटिक अल्कोहल के लिए आइसोमेरिक हैं, अर्थात। सामान्य आणविक सूत्र C n H 2n-6 O भी हैं।
amines
Aminami अमोनिया का डेरिवेटिव, जिसमें एक, दो या सभी तीन हाइड्रोजन परमाणुओं को हाइड्रोकार्बन कट्टरपंथी द्वारा प्रतिस्थापित किया जाता है।
एमाइन जिसमें केवल एक हाइड्रोजन परमाणु को हाइड्रोकार्बन रेडिकल द्वारा प्रतिस्थापित किया जाता है, अर्थात्। सामान्य सूत्र वाले R-NH 2 को कहा जाता है प्राथमिक अमीन.
एमाइन जिसमें दो हाइड्रोजन परमाणुओं को हाइड्रोकार्बन रेडिकल द्वारा प्रतिस्थापित किया जाता है, कहा जाता है द्वितीयक अमाइन... द्वितीयक अमाइन सूत्र को R-NH-R 'के रूप में लिखा जा सकता है। इस मामले में, कट्टरपंथी आर और आर 'या तो एक ही या अलग हो सकते हैं। उदाहरण के लिए:
यदि अमाइन में नाइट्रोजन परमाणु में हाइड्रोजन परमाणु नहीं होते हैं, अर्थात्। अमोनिया अणु के सभी तीन हाइड्रोजन परमाणुओं को एक हाइड्रोकार्बन कट्टरपंथी द्वारा प्रतिस्थापित किया जाता है, फिर ऐसे अमाइन कहा जाता है तृतीयक amines... सामान्य शब्दों में, तृतीयक अमीन सूत्र को निम्नानुसार लिखा जा सकता है:
इस मामले में, कट्टरपंथी आर, आर ', आर' 'या तो पूरी तरह से समान या सभी तीन अलग हो सकते हैं।
प्राथमिक, माध्यमिक और तृतीयक संतृप्त अमाइन का सामान्य आणविक सूत्र C n H 2 n +3 N है।
केवल एक असंतृप्त पदार्थ के साथ सुगंधित amines में सामान्य सूत्र C n H 2 n -5 N होता है
एल्डिहाइड और किटोन
एल्डीहाइड हाइड्रोकार्बन के डेरिवेटिव को कहा जाता है, जिसमें प्राथमिक कार्बन परमाणु में दो हाइड्रोजन परमाणुओं को एक ऑक्सीजन परमाणु द्वारा प्रतिस्थापित किया जाता है, अर्थात। संरचना में हाइड्रोकार्बन का व्युत्पन्न होता है जिसमें एक एल्डिहाइड समूह होता है -CH \u003d O एल्डिहाइड के लिए सामान्य सूत्र आर-सीएच \u003d ओ के रूप में लिखा जा सकता है। उदाहरण के लिए:
ketones हाइड्रोकार्बन के डेरिवेटिव को कहा जाता है, जिसमें माध्यमिक कार्बन परमाणु में दो हाइड्रोजन परमाणुओं को ऑक्सीजन परमाणु द्वारा प्रतिस्थापित किया जाता है, अर्थात। की संरचना में यौगिकों जिसमें एक कार्बोनिल समूह है -सी (ओ) -।
केटोन्स के लिए सामान्य सूत्र को R-C (O) -R 'लिखा जा सकता है। इस मामले में, कट्टरपंथी आर, आर 'या तो एक ही या अलग हो सकता है।
उदाहरण के लिए:
| प्रोपेन वह | बुटान वह |
जैसा कि आप देख सकते हैं, एल्डीहाइड और कीटोन संरचना में बहुत समान हैं, लेकिन वे अभी भी कक्षाओं के रूप में प्रतिष्ठित हैं, क्योंकि उनके रासायनिक गुणों में महत्वपूर्ण अंतर है।
संतृप्त कीटोन्स और एल्डिहाइड का सामान्य आणविक सूत्र समान है और इसका रूप C n H 2 n O है
कार्बोक्जिलिक एसिड
कार्बोक्जिलिक एसिड हाइड्रोकार्बन का डेरिवेटिव कहा जाता है जिसमें एक कार्बोक्सिल समूह -COOH होता है।
यदि किसी अम्ल में दो कार्बोक्सिल समूह होते हैं, तो इस अम्ल को कहा जाता है डाइकारबॉक्सिलिक एसिड.
संतृप्त मोनोकारबॉक्सिलिक एसिड (एक समूह -COOH के साथ) का सामान्य आणविक सूत्र है C n H 2 n 2 2
एरोमैटिक मोनोकारबॉक्सिलिक एसिड का सामान्य सूत्र C n H 2 n -8 O 2 है
ईथर
पंख -कार्बनिक यौगिक जिसमें दो हाइड्रोकार्बन मूलक अप्रत्यक्ष रूप से एक ऑक्सीजन परमाणु के माध्यम से जुड़े होते हैं, अर्थात्। फॉर्म का फॉर्मूला R-O-R 'है। इस मामले में, कट्टरपंथी आर और आर 'या तो एक ही या अलग हो सकते हैं।
उदाहरण के लिए:
संतृप्त पंखों के लिए सामान्य सूत्र संतृप्त मोनोहाइड्रिक अल्कोहल के लिए समान है, अर्थात। सी एन एच 2 एन +1 ओएच या सी एन एच 2 एन +2 ओ।
एस्टर
एस्टर कार्बनिक कार्बोक्जिलिक एसिड पर आधारित यौगिकों का एक वर्ग है, जिसमें हाइड्रॉक्सिल समूह में हाइड्रोजन परमाणु को हाइड्रोकार्बन कट्टरपंथी आर द्वारा प्रतिस्थापित किया जाता है। सामान्य रूप में एस्टर का सूत्र निम्नानुसार लिखा जा सकता है:
उदाहरण के लिए:
नाइट्रो यौगिक
नाइट्रो यौगिक - हाइड्रोकार्बन के डेरिवेटिव, जिसमें एक या एक से अधिक हाइड्रोजन परमाणुओं को नाइट्रो समूह द्वारा प्रतिस्थापित किया जाता है -नो 2।
एक नाइट्रो समूह के साथ नाइट्रो यौगिकों की सीमा सामान्य आणविक सूत्र C n H 2 n +1 NO 2 है
अमीनो अम्ल
एक साथ दो कार्यात्मक समूहों - अमीनो एनएच 2 और कार्बोक्सिल - सीओओएच में उनकी संरचना में होने वाले यौगिक। उदाहरण के लिए,
NH 2 -CH 2 -COOH
एक कार्बोक्सिल और एक एमिनो समूह के साथ अमीनो एसिड की सीमा नाइट्रो यौगिकों को सीमित करने के लिए आइसोमेरिक है, अर्थात। क्योंकि उनके पास सामान्य आणविक सूत्र C n H 2 n +1 NO 2 है
कार्बनिक पदार्थों के वर्गीकरण के लिए यूएसई कार्यों में, कार्बन कंकाल की संरचनात्मक विशेषताओं और कुछ कार्यात्मक समूहों की उपस्थिति को जानते हुए, विभिन्न प्रकार के यौगिकों के समरूप श्रृंखला के सामान्य आणविक सूत्रों को लिखने में सक्षम होना महत्वपूर्ण है। विभिन्न वर्गों के कार्बनिक यौगिकों के सामान्य आणविक सूत्रों को निर्धारित करने का तरीका जानने के लिए, इस विषय पर सामग्री उपयोगी होगी।
कार्बनिक यौगिकों का नामकरण
यौगिकों की संरचना और रासायनिक गुणों की विशेषताएं नामकरण में परिलक्षित होती हैं। मुख्य प्रकार की वस्तुओं को माना जाता है व्यवस्थित तथा तुच्छ.
व्यवस्थित नामकरण वास्तव में एल्गोरिदम को निर्धारित करता है, जिसके अनुसार किसी विशेष नाम को कार्बनिक पदार्थों के अणु की संरचनात्मक विशेषताओं के अनुसार कड़ाई से संकलित किया जाता है या, मोटे तौर पर इसके संरचनात्मक सूत्र।
व्यवस्थित नामकरण के अनुसार कार्बनिक यौगिकों के नाम संकलित करने के नियमों पर विचार करें।
व्यवस्थित नामकरण के अनुसार कार्बनिक पदार्थों के नामों का संकलन करते समय, सबसे महत्वपूर्ण बात यह है कि सबसे लंबी कार्बन श्रृंखला में कार्बन परमाणुओं की संख्या को सही ढंग से निर्धारित करना या एक चक्र में कार्बन परमाणुओं की संख्या की गणना करना।
मुख्य कार्बन श्रृंखला में कार्बन परमाणुओं की संख्या के आधार पर, यौगिकों के नाम में एक अलग जड़ होगी:
|
मुख्य कार्बन श्रृंखला में C परमाणुओं की संख्या |
नाम जड़ |
|
prop- |
|
|
pent- |
|
|
hex- |
|
|
hept- |
|
|
dec (c) - |
नामों को संकलित करते समय ध्यान में रखा गया दूसरा महत्वपूर्ण घटक कई बांड या कार्यात्मक समूहों की उपस्थिति / अनुपस्थिति है, जो ऊपर तालिका में सूचीबद्ध हैं।
आइए एक पदार्थ को एक नाम देने की कोशिश करें जिसमें एक संरचनात्मक सूत्र है:
1. इस अणु की मुख्य (और केवल) कार्बन श्रृंखला में 4 कार्बन परमाणु होते हैं, इसलिए इस नाम में मूल जड़ होगी लेकिन-;
2. कार्बन कंकाल में एक से अधिक बांड नहीं होते हैं, इसलिए, शब्द की जड़ के बाद जो प्रत्यय होना चाहिए, वह एक-जैसा होगा, जैसा कि एसाइक्लिक हाइड्रोकार्बन (एल्केन्स) को सीमित करता है;
3. कार्यात्मक समूह की उपस्थिति -OH, बशर्ते कि कोई और अधिक वरिष्ठ कार्यात्मक समूह नहीं हैं, आइटम 2 से रूट और प्रत्यय के बाद जोड़ता है। एक और प्रत्यय "ओल" है;
4. कई बांड या कार्यात्मक समूहों वाले अणुओं में, मुख्य श्रृंखला के कार्बन परमाणुओं की संख्या अणु के किनारे से शुरू होती है, जिसके वे करीब हैं।
आइए एक और उदाहरण देखें:
मुख्य कार्बन श्रृंखला में चार कार्बन परमाणुओं की उपस्थिति हमें बताती है कि नाम की जड़ "लेकिन" है, और कई बांडों की अनुपस्थिति प्रत्यय "-an" को इंगित करती है, जो रूट के तुरंत बाद का पालन करेगी। इस यौगिक में पुराना समूह कार्बोक्सिल है, जो इस पदार्थ के संबंधित को कार्बोक्जिलिक एसिड के वर्ग में निर्धारित करता है। इसलिए, नाम का अंत "-ओइक एसिड" होगा। दूसरे कार्बन परमाणु में एक एमिनो समूह है NH 2 -इसलिए, यह पदार्थ अमीनो एसिड के अंतर्गत आता है। इसके अलावा तीसरे कार्बन परमाणु में, हम हाइड्रोकार्बन कट्टरपंथी मिथाइल देखते हैं ( सीएच 3 -)। इसलिए, व्यवस्थित नामकरण के अनुसार, इस यौगिक को 2-एमिनो-3-मिथाइलबुटानोइक एसिड कहा जाता है।
तुच्छ नामकरण, एक नियम के रूप में, एक नियम के रूप में, किसी पदार्थ की संरचना के साथ कोई संबंध नहीं है, लेकिन मुख्य रूप से इसकी उत्पत्ति, साथ ही साथ रासायनिक या भौतिक गुणों के कारण है।
| सूत्र | व्यवस्थित नामकरण | तुच्छ नाम |
| हाइड्रोकार्बन | ||
| सीएच 4 | मीथेन | दलदली गैस |
| सीएच 2 \u003d सीएच 2 | ethen | एथिलीन |
| सीएच 2 \u003d सीएच-सीएच 3 | propene | प्रोपलीन |
| CH≡CH | ethine | एसिटिलीन |
| सीएच 2 \u003d सीएच-सीएच \u003d सीएच 2 | butadiene-1,3 | divinyl |
| 2-methylbutadiene-1,3 | आइसोप्रेन | |
| methylbenzene | टोल्यूनि | |
| 1,2-dimethylbenzene | ऑर्थो-xylene (के बारे में-xylene) |
|
| 1,3-dimethylbenzene | मेटा-xylene (म-xylene) |
|
| 1,4-dimethylbenzene | जोड़ा-xylene (पी-xylene) |
|
| vinylbenzene | स्टाइरीन | |
| अल्कोहल | ||
| सीएच 3 ओएच | मेथनॉल | मिथाइल अल्कोहल, लकड़ी शराब |
| सीएच 3 सीएच 2 ओएच | इथेनॉल | इथेनॉल |
| CH 2 \u003d CH-CH 2 -OH | propene-2-ol-1 | अल्ली अल्कोहल |
| ethanediol-1,2 | इथाइलीन ग्लाइकॉल | |
| propanetriol-1,2,3 | ग्लिसरॉल | |
| फिनोल (Hydroxybenzene) |
पांगविक अम्ल | |
| 1-हाइड्रोक्सी-2-methylbenzene | ऑर्थो-cresol (के बारे में-cresol) |
|
| 1-हाइड्रोक्सी-3-methylbenzene | मेटा-cresol (म-cresol) |
|
| 1-हाइड्रोक्सी-4-methylbenzene | जोड़ा-cresol (पी-cresol) |
|
| phenylmethanol | बेंजाइल अल्कोहल | |
| एल्डिहाइड और किटोन | ||
| methanal | formaldehyde | |
| ethanal | एसिटालडिहाइड, एसिटालडिहाइड | |
| propenal | ऐक्रेलिक एल्डिहाइड, एक्रोलिन | |
| benzaldehyde | बेंजोइक एल्डिहाइड | |
| propanone | एसीटोन | |
| कार्बोक्जिलिक एसिड | ||
| (HCOOH) | मिथानोइक अम्ल | फॉर्मिक एसिड (लवण और एस्टर - फॉर्मेट्स) |
| (सीएच 3 कोह) | इथेनिक एसिड | सिरका अम्ल (लवण और एस्टर - एसीटेट) |
| (सीएच 3 सीएच 2 सीओओएच) | प्रोपोनिक एसिड | प्रोपियॉनिक अम्ल (लवण और एस्टर - प्रोपियोनेट्स) |
| C 15 H 31 COOH | हेक्साडेकोनिक एसिड | पामिटिक एसिड (लवण और एस्टर - पामिटेट) |
| C 17 H 35 COOH | ऑक्टाडेकोनिक एसिड | स्टीयरिक अम्ल (लवण और एस्टर - stearates) |
| प्रोपेनोइक एसिड | एक्रिलिक एसिड (लवण और एस्टर - एक्रिलेट्स) |
|
| HOOC-COOH | एथेनेडिओइक एसिड | ऑक्सालिक एसिड (लवण और एस्टर - ऑक्सालेट) |
| 1,4-बेन्ज़ेंडीकारबॉक्सिलिक एसिड | terephthalic acid | |
| एस्टर | ||
| HCOOCH 3 | methylmetanoate | मिथाइल फॉर्मेट, म्यूरिक एसिड मिथाइल एस्टर |
| सीएच 3 कोच 3 | methylethanoate | मिथाइल एसीटेट, एसिटिक एसिड मिथाइल एस्टर |
| सीएच 3 सीओओसी 2 एच 5 | एथिल एथानोएट | इथाइल एसीटेट, इथाइल एसीटेट |
| सीएच 2 \u003d सीएच-कोच 3 | मिथाइल प्रोपेनोएट | मिथाइल एक्रिलाट, ऐक्रेलिक एसिड मिथाइल एस्टर |
| नाइट्रोजन यौगिक | ||
| aminobenzene, phenylamine |
रंगों का रासायनिक आधार | |
| NH 2 -CH 2 -COOH | एमिनोइथेनिक एसिड | ग्लाइसिन, एमिनोएसिटिक एसिड |
| 2-अमीनोप्रोपोनिक एसिड | alanine | |
सभी पदार्थ जिनमें कार्बोनेट, कार्बाइड, साइनाइड, थायोसाइनेट और कार्बोनिक एसिड के अलावा कार्बन परमाणु होते हैं, वे कार्बनिक यौगिक होते हैं। इसका मतलब है कि वे एंजाइम या अन्य प्रतिक्रियाओं के माध्यम से कार्बन परमाणुओं से जीवित जीवों द्वारा बनाए जाने में सक्षम हैं। आज, कई कार्बनिक पदार्थों को कृत्रिम रूप से संश्लेषित किया जा सकता है, जो दवा और फार्माकोलॉजी के विकास के साथ-साथ उच्च शक्ति वाले बहुलक और मिश्रित सामग्रियों के निर्माण की अनुमति देता है।
कार्बनिक यौगिकों का वर्गीकरण
कार्बनिक यौगिक पदार्थों के सबसे कई वर्ग हैं। यहां लगभग 20 प्रकार के पदार्थ हैं। वे रासायनिक गुणों में भिन्न हैं, भौतिक गुणों में भिन्न हैं। उनका पिघलने बिंदु, द्रव्यमान, अस्थिरता और घुलनशीलता, साथ ही साथ सामान्य परिस्थितियों में एकत्रीकरण की उनकी स्थिति भी भिन्न होती है। उनमें से:
- हाइड्रोकार्बन (एल्केन्स, एल्केनीज़, एल्केनीज़, एल्केडिएन्स, साइक्लोकलेन, एरोमैटिक हाइड्रोकार्बन);
- एल्डीहाइड;
- कीटोन;
- अल्कोहल (डायटोमिक, मोनोहाइड्रिक, पॉलीहाइड्रिक);
- ईथर;
- एस्टर;
- कार्बोक्जिलिक एसिड;
- amines;
- अमीनो अम्ल;
- कार्बोहाइड्रेट;
- वसा;
- प्रोटीन;
- बायोपॉलिमर और सिंथेटिक पॉलिमर।
यह वर्गीकरण रासायनिक संरचना की विशेषताओं और विशिष्ट परमाणु समूहों की उपस्थिति को दर्शाता है जो किसी दिए गए पदार्थ के गुणों में अंतर निर्धारित करते हैं। सामान्य तौर पर, वर्गीकरण, जो कार्बन कंकाल के विन्यास पर आधारित होता है, जो रासायनिक इंटरैक्शन की विशेषताओं को ध्यान में नहीं रखता है, अलग दिखता है। इसके प्रावधानों के अनुसार, कार्बनिक यौगिकों में विभाजित हैं:
- स्निग्ध यौगिक;
- सुगंधित पदार्थ;
- विषमलैंगिक पदार्थ।
कार्बनिक यौगिकों के इन वर्गों में पदार्थों के विभिन्न समूहों में आइसोमर्स हो सकते हैं। आइसोमर्स के अलग-अलग गुण हैं, हालांकि उनकी परमाणु संरचना समान हो सकती है। यह ए.एम. बटलरोव द्वारा निर्धारित प्रावधानों से निम्नानुसार है। इसके अलावा, कार्बनिक यौगिकों की संरचना का सिद्धांत कार्बनिक रसायन विज्ञान में सभी अनुसंधानों के लिए मार्गदर्शक आधार है। इसे मेंडेलीव के आवधिक कानून के समान स्तर पर रखा गया है।
रासायनिक संरचना की बहुत अवधारणा ए.एम. बटलरोव द्वारा शुरू की गई थी। यह 19 सितंबर, 1861 को रसायन विज्ञान के इतिहास में दिखाई दिया। पहले, विज्ञान में अलग-अलग राय थी, और कुछ वैज्ञानिकों ने अणुओं और परमाणुओं की उपस्थिति से पूरी तरह से इनकार किया। इसलिए, कार्बनिक और अकार्बनिक रसायन विज्ञान में कोई आदेश नहीं था। इसके अलावा, कोई नियमितता नहीं थी जिसके द्वारा कोई विशिष्ट पदार्थों के गुणों का न्याय कर सकता था। इसके अलावा, ऐसे यौगिक थे, जो एक ही रचना के साथ, विभिन्न गुणों को दर्शाते थे।

एएम बटलरोव के बयानों ने बड़े पैमाने पर रसायन विज्ञान के विकास को सही दिशा में निर्देशित किया और इसके लिए एक ठोस आधार तैयार किया। इसके माध्यम से, संचित तथ्यों, कुछ पदार्थों के रासायनिक या भौतिक गुणों, प्रतिक्रियाओं में उनके प्रवेश के पैटर्न, और इसी तरह व्यवस्थित करना संभव था। यहां तक \u200b\u200bकि यौगिकों को प्राप्त करने के तरीकों की भविष्यवाणी और कुछ सामान्य गुणों की उपस्थिति इस सिद्धांत के लिए संभव हो गई। और सबसे महत्वपूर्ण बात, ए एम बटलरोव ने दिखाया कि एक पदार्थ के अणु की संरचना को विद्युत इंटरैक्शन के संदर्भ में समझाया जा सकता है।
कार्बनिक पदार्थों की संरचना के सिद्धांत का तर्क
1861 से रसायन विज्ञान में, कई ने एक परमाणु या एक अणु के अस्तित्व को खारिज कर दिया, जैविक यौगिकों का सिद्धांत वैज्ञानिक दुनिया के लिए एक क्रांतिकारी प्रस्ताव बन गया। और चूंकि ए.एम. बटलरोव खुद भौतिकवादी संदर्भों से आगे बढ़ते हैं, इसलिए वे कार्बनिक पदार्थों के बारे में दार्शनिक विचारों का खंडन करने में कामयाब रहे।
वह यह दिखाने में सक्षम था कि आणविक संरचना को रासायनिक प्रतिक्रियाओं के माध्यम से अनुभवजन्य रूप से पहचाना जा सकता है। उदाहरण के लिए, किसी भी कार्बोहाइड्रेट की संरचना को एक निश्चित मात्रा में जलाने और परिणामस्वरूप पानी और कार्बन डाइऑक्साइड की गिनती करके निर्धारित किया जा सकता है। एक अमाइन अणु में नाइट्रोजन की मात्रा की गणना दहन के दौरान गैसों की मात्रा और आणविक नाइट्रोजन की रासायनिक मात्रा के विमोचन से भी की जाती है।
यदि हम संरचना के आधार पर, विपरीत दिशा में, रासायनिक संरचना के बारे में बटलरोव के निर्णयों पर विचार करते हैं, तो एक नया निष्कर्ष खुद पता चलता है। अर्थात्: किसी पदार्थ की रासायनिक संरचना और संरचना को जानना, कोई व्यक्ति इसके गुणों को अनुभव कर सकता है। लेकिन सबसे महत्वपूर्ण बात, बटलरोव ने स्पष्ट किया कि कार्बनिक पदार्थों में बड़ी संख्या में ऐसे पदार्थ होते हैं जो विभिन्न गुणों को प्रदर्शित करते हैं, लेकिन उनकी रचना समान होती है।
सिद्धांत के सामान्य प्रावधान
कार्बनिक यौगिकों को ध्यान में रखते हुए और जांच करते हुए, बटलरोव ए.एम. ने कुछ सबसे महत्वपूर्ण कानूनों की कटौती की। उन्होंने उन्हें कार्बनिक मूल के रसायनों की संरचना को समझाते हुए सिद्धांत के प्रावधानों में जोड़ा। सिद्धांत इस प्रकार है:
- कार्बनिक पदार्थों के अणुओं में, परमाणु एक कड़ाई से परिभाषित अनुक्रम में एक दूसरे से जुड़े होते हैं, जो कि वैधता पर निर्भर करता है;
- रासायनिक संरचना प्रत्यक्ष क्रम है जिसके अनुसार कार्बनिक अणुओं में परमाणु जुड़े हुए हैं;
- रासायनिक संरचना एक कार्बनिक यौगिक के गुणों को निर्धारित करती है;
- एक ही मात्रात्मक रचना के साथ अणुओं की संरचना के आधार पर, किसी पदार्थ के विभिन्न गुणों की उपस्थिति संभव है;
- रासायनिक यौगिक के निर्माण में भाग लेने वाले सभी परमाणु समूह एक दूसरे पर परस्पर प्रभाव डालते हैं।

इस सिद्धांत के सिद्धांतों के अनुसार कार्बनिक यौगिकों के सभी वर्गों का निर्माण किया जाता है। नींव रखने के बाद, बटलरोव ए.एम. रसायन विज्ञान के क्षेत्र के रूप में विस्तार करने में सक्षम थे। उन्होंने बताया कि इस तथ्य के कारण कि कार्बन कार्बनिक पदार्थों में चार की वैधता प्रदर्शित करता है, इन यौगिकों की विविधता निर्धारित की जाती है। कई सक्रिय परमाणु समूहों की उपस्थिति एक निश्चित वर्ग के लिए एक पदार्थ से संबंधित निर्धारित करती है। और यह विशिष्ट परमाणु समूहों (कट्टरपंथी) की उपस्थिति के कारण है जो भौतिक और रासायनिक गुण प्रकट होते हैं।

हाइड्रोकार्बन और उनके डेरिवेटिव
कार्बन और हाइड्रोजन के ये कार्बनिक यौगिक समूह के सभी पदार्थों के बीच संरचना में सबसे सरल हैं। वे अल्केन्स और साइक्लोअल्केन (संतृप्त हाइड्रोकार्बन), अल्केन्स, अल्केडिएन्स और अल्कैट्रीन्स, एल्केनीज़ (असंतृप्त हाइड्रोकार्बन), साथ ही साथ सुगंधित पदार्थों के एक उपवर्ग का प्रतिनिधित्व करते हैं। अल्कनेस में, सभी कार्बन परमाणु केवल एक ही सी-सी बॉन्ड से जुड़े होते हैं, यही कारण है कि हाइड्रोकार्बन संरचना में एक भी एच परमाणु को शामिल नहीं किया जा सकता है।
असंतृप्त हाइड्रोकार्बन में, हाइड्रोजन को डबल सी \u003d सी बांड की साइट पर शामिल किया जा सकता है। साथ ही, C-C बॉन्ड ट्रिपल (क्षार) हो सकता है। यह इन पदार्थों को विभिन्न प्रकार के प्रतिक्रियाओं में प्रवेश करने की अनुमति देता है जो कि कट्टरपंथियों की कमी या वृद्धि से जुड़े होते हैं। प्रतिक्रियाओं में प्रवेश करने की अपनी क्षमता का अध्ययन करने की सुविधा के लिए अन्य सभी पदार्थों को हाइड्रोकार्बन के वर्गों में से एक के डेरिवेटिव के रूप में माना जाता है।

अल्कोहल
हाइड्रोकार्बन की तुलना में अल्कोहल को कार्बनिक रासायनिक यौगिक कहा जाता है। जीवित कोशिकाओं में एंजाइमेटिक प्रतिक्रियाओं के परिणामस्वरूप उन्हें संश्लेषित किया जाता है। सबसे विशिष्ट उदाहरण किण्वन द्वारा ग्लूकोज से इथेनॉल का संश्लेषण है।
उद्योग में, एल्कोहल हाइड्रोकार्बन के हेलोजन डेरिवेटिव से प्राप्त किया जाता है। हाइड्रॉक्सिल समूह के लिए हलोजन परमाणु के प्रतिस्थापन के परिणामस्वरूप, अल्कोहल का निर्माण होता है। मोनोहाइड्रिक अल्कोहल में केवल एक हाइड्रॉक्सिल समूह, पॉलीहाइड्रिक अल्कोहल - दो या अधिक होते हैं। डायहाइड्रिक अल्कोहल का एक उदाहरण एथिलीन ग्लाइकॉल है। पॉलीहाइड्रिक अल्कोहल ग्लिसरीन है। अल्कोहल का सामान्य सूत्र आर-ओएच (आर एक कार्बन श्रृंखला है)।
एल्डिहाइड और किटोन
अल्कोहल (हाइड्रॉक्सिल) समूह से हाइड्रोजन के उन्मूलन से जुड़े कार्बनिक यौगिकों की प्रतिक्रिया के बाद अल्कोहल में प्रवेश होता है, ऑक्सीजन और कार्बन के बीच एक दोहरा बंधन बंद हो जाता है। यदि यह प्रतिक्रिया टर्मिनल कार्बन परमाणु में स्थित शराब समूह में होती है, तो इसके परिणामस्वरूप, यह एक एल्डिहाइड बनाता है। यदि शराब के साथ कार्बन परमाणु कार्बन श्रृंखला के अंत में स्थित नहीं है, तो निर्जलीकरण प्रतिक्रिया का परिणाम कीटोन का उत्पादन होता है। केटोन्स का सामान्य सूत्र R-CO-R है, aldehydes R-COH (R श्रृंखला का हाइड्रोकार्बन रेडिकल है)।

पंख (सरल और जटिल)
इस वर्ग के कार्बनिक यौगिकों की रासायनिक संरचना जटिल है। पंखों को दो अल्कोहल अणुओं के बीच प्रतिक्रिया उत्पादों के रूप में माना जाता है। जब पानी उनसे अलग हो जाता है, तो नमूना यौगिक R-O-R बनता है। प्रतिक्रिया तंत्र: एक शराब से हाइड्रोजन प्रोटॉन का उन्मूलन और दूसरी शराब से हाइड्रॉक्सिल समूह।
एस्टर शराब और एक कार्बनिक कार्बोक्जिलिक एसिड के बीच प्रतिक्रिया के उत्पाद हैं। प्रतिक्रिया तंत्र: दोनों अणुओं के शराब और कार्बोक्जिलिक समूहों से पानी का उन्मूलन। हाइड्रोजन को एसिड (हाइड्रॉक्सिल समूह द्वारा) से अलग किया जाता है, और ओएच समूह को शराब से अलग किया जाता है। परिणामस्वरूप यौगिक को आर-सीओ-ओ-आर के रूप में दर्शाया गया है, जहां बीच आर का मतलब है कट्टरपंथी - बाकी कार्बन श्रृंखला।
कार्बोक्जिलिक एसिड और एमाइन
कार्बोक्जिलिक एसिड विशेष पदार्थ होते हैं जो कोशिका के कामकाज में महत्वपूर्ण भूमिका निभाते हैं। कार्बनिक यौगिकों की रासायनिक संरचना इस प्रकार है: एक हाइड्रोकार्बन कट्टरपंथी (R) जिसके साथ एक कार्बोक्सिल समूह जुड़ा हुआ है (-COOH)। कार्बोक्सिल समूह केवल अत्यधिक कार्बन परमाणु पर स्थित हो सकता है, क्योंकि (-OH) समूह में सी की वैधता 4 है।
अमाइन सरल यौगिक हैं जो हाइड्रोकार्बन से प्राप्त होते हैं। यहां किसी भी कार्बन परमाणु में एक अमाइन रेडिकल (-NH2) होता है। प्राथमिक अमीन होते हैं जिसमें एक समूह (-NH2) एक कार्बन (सामान्य सूत्र R-NH2) से जुड़ा होता है। माध्यमिक amines नाइट्रोजन को दो कार्बन परमाणुओं (सूत्र R-NH-R) के साथ मिलाते हैं। तृतीयक अमाइन में, नाइट्रोजन तीन कार्बन परमाणुओं (R3N) से जुड़ा होता है, जहां पी एक कट्टरपंथी, एक कार्बन श्रृंखला है।
अमीनो अम्ल
अमीनो एसिड जटिल यौगिक हैं जो कार्बनिक मूल के अमाइन और एसिड दोनों के गुणों को प्रदर्शित करते हैं। कार्बोक्सिल समूह के संबंध में अमीन समूह के स्थान के आधार पर, उनमें से कई प्रकार हैं। सबसे महत्वपूर्ण हैं अल्फा एमिनो एसिड। यहां कार्बन समूह पर अमाइन समूह स्थित है, जिससे कार्बोक्सिल जुड़ा हुआ है। यह आपको पेप्टाइड बॉन्ड बनाने और प्रोटीन को संश्लेषित करने की अनुमति देता है।

कार्बोहाइड्रेट और वसा
कार्बोहाइड्रेट एल्डीहाइड अल्कोहल या केटलॉर्क्स हैं। ये एक रैखिक या चक्रीय संरचना के साथ यौगिक हैं, साथ ही पॉलिमर (स्टार्च, सेलूलोज़, और अन्य)। कोशिका में उनकी सबसे महत्वपूर्ण भूमिका संरचनात्मक और ऊर्जावान होती है। वसा, या लिपिड, समान कार्य करते हैं, केवल अन्य जैव रासायनिक प्रक्रियाओं में भाग लेते हैं। रासायनिक संरचना के संदर्भ में, वसा कार्बनिक अम्ल और ग्लिसरॉल का एक एस्टर है।
